Vaccination
Vaccination
Le territoire de la CPTS montre des statistiques vaccinales légèrement plus favorable par rapport au reste de la région :
Concernant la vaccination antigrippale, 53,2% des plus de 65 ans sont vaccinés (vs 51,2% sur la région et 53,1% en France). Il en va de même pour les patients à risque : 28,6% sur le territoire (vs 27,9% en région PACA et 1,2% sur le reste de la France) ; La tendance est similaire pour la vaccination ROR et méningocoque C respectivement de 81,3% (vs 74,7% en PACA et 79,4% en France) et 85,8% pour le méningocoque C (vs 82,3% et 85,3% sur le reste de la France). En ce qui concerne la couverture vaccinale contre le pneumocoque, si le Var est sensiblement au même taux que la région PACA (90% vs 89,5%), elle est un peu inférieure à la moyenne nationale (92,2 %)
Rappel
Pneumonies à Pneumocoques
Streptococcus pneumoniae est une bactérie commensale du rhinopharynx de l’Homme hautement recombinante (plus de 90 sérotypes connus) Avec 15 millions d’infections invasives et 1,5 millions de décès par an dans le monde, streptococcus pneumoniae représente un problème majeur de santé publique à l’échelle mondiale.
Si tous les sérotypes de pneumocoques n’ont pas la même capacité à coloniser le rhinopharynx ou à provoquer des infections, aucun pneumocoque ne peut être considéré comme non pathogène. Streptococcus pneumoniae est un redoutable pathogène : Il est le principal agent étiologique des pneumonies aigües communautaires et des méningites.
Le risque d’infection à pneumocoque est particulièrement élevé chez les enfants dans leurs trois premières années de vie, chez les sujets âgés de plus de 65 ans et à tout âge chez les personnes présentant une immunodépression.
Depuis 2001, l’étude des sérotypes et de la sensibilité aux antibiotiques montre un effet direct et indirect de la vaccination des enfants de moins de 2 ans par le vaccin conjugué (7- valent fin 2002, remplacé par le 13-valent en juin 2010) qui a joué un rôle important dans la diminution de l’incidence des infections invasives à pneumocoques.
L’effet du vaccin conjugué est net : les infections à sérotypes vaccinaux continuent de diminuer, excepté les infections liées au sérotype 3.
Qui porte l’agent pathogène du méningocoque et du pneumocoque ?
Illustration simplifiée du rôle pivot des adolescents dans l’épidémiologie de la méningococcie par rapport à d’autres agents pathogènes qui sont également à l’origine de maladies invasives.
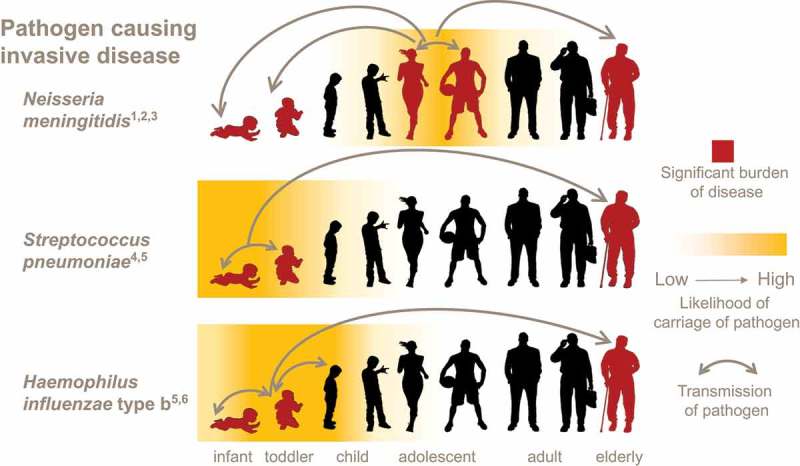
Source : Volker Vetter , Roger Baxter , Gülhan Denizer , Marco AP Sáfadi , Sven-Arne Silfverdal, Andrew Vyse , et Ray Borrow – Vacciner systématiquement les adolescents contre le méningocoque: cibler la transmission et la maladie Vaccins Rev Expert. 3 mai 2016; 15 (5): 641–658.
Les infections à Pneumocoques : Rappels et généralités :
Les poumons sont la porte d’entrée de 79% des infections invasives.
On note une admission en services de réanimation dans 39% des cas
On note un nombre de décès hospitalier représentant 16,4 à 21% des cas à 30 jours
La durée médiane de séjour est de 10 jours
Source : Epidemiology and Prevention of Vaccine-Preventable Diseases, 11th edition, Revised May 2009
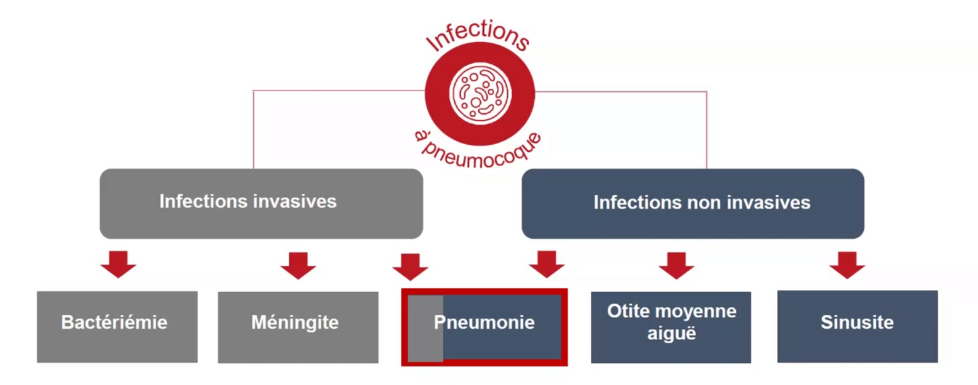
Une étude populationnelle prospective de toutes les hospitalisations pour Pneumonies Aigües Communautaires (PAC) a été menée pendant 2 ans (juin 2014 – mai 2016) chez les adultes de Louisville, Ky, USA, avec comme critères d’inclusion :
- ≥ 18 ans
- 1/ Infiltrat pulmonaire diagnostiqué par radiographie thoracique et certifié
- 2/ Au moins un critère clinique
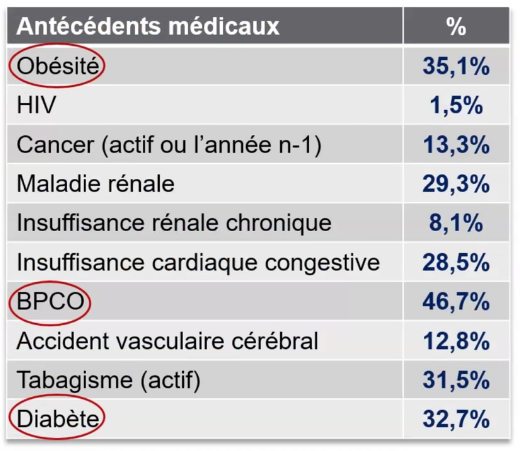
Sur une population de 587 499 adultes, il a été identifié 7 449 PAC hospitalisées. L’âge médian de la population concernée est de 68 ans
Il est retrouvé dans de nombreux cas des antécédents médicaux dont 3 pathologies se retrouvent dans plus de 30 % des cas : L’obésité, la BPCO et le Diabète.
Source : Ramirez JA & al. Adults Hospitalized With Pneumonia in the United States: Incidence, Epidemiology, and Mortality, Clin Infect Dis. 2017 Nov 13;65(11):1806-1812. Doi: 10.1093/cid/cix647..
Par ailleurs, il est établit qu’un patient cumulant 2 comorbidités à risque présente un risque similaire à celui des patients à haut risque.
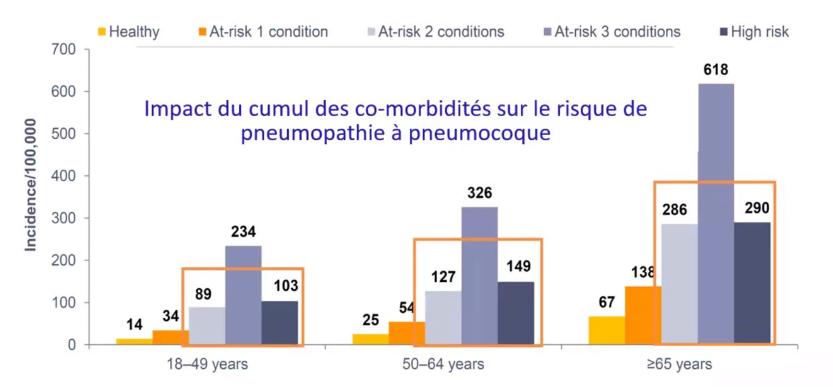
Source : Shea M. and al, Rates of Pneumococcal Disease in Adults With Chronic Medical Conditions, 2014, Open Forum Infectious Diseases
Il est également à noter le risque relatif d’infections à pneumocoque selon la maladie auto-immune :
Source : Wotton, J Epidemiol Community Health april 2012
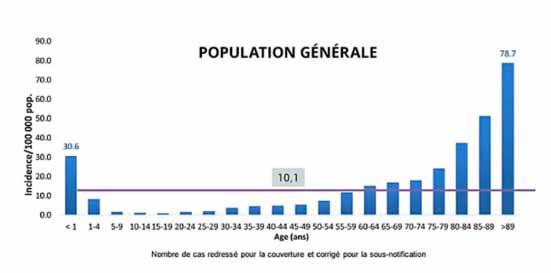
Les infections invasives à pneumocoques ont une incidence élevée aux âges extrêmes de la vie : immaturité du système immunitaire avant l’âge de 2 ans et immunosénescence associée ou non à des comorbidités après 50 ans
Source : EPIBAC 2018, Santé Publique France.
Vaccination antipneumococcique :
Les recommandations vaccinales contre les infections à pneumocoque chez les adultes ont été actualisées par un avis du Haut Conseil de la santé publique daté du 10 mars 2017 (et publié le 25 avril 2017) au vu des nouvelles données d’efficacité du vaccin pneumococcique conjugué 13-valent Prevenar 13.
Cette actualisation des recommandations vaccinales de 2017 a été établie au vu des données d’une étude de grande ampleur portant sur l’efficacité du vaccin Prevenar 13 dans la prévention des pneumonies à pneumocoque chez les personnes de 65 ans et plus : l’étude CAPiTA.
L’étude CAPiTA (Community-Acquired Pneumonia Immunization Trial in Adults) est une étude randomisée en double aveugle, c’est-à-dire avec un niveau de preuve élevée, qui a été conduite aux Pays-Bas auprès de 85 000 personnes âgées de 65 ans et plus. Ces personnes étaient réparties en deux groupes de taille équivalente : le groupe des personnes vaccinées recevait une dose de Prevenar 13, tandis que le groupe témoin recevait un placebo. L’efficacité du vaccin Prevenar 13 a été mesurée en comparant le nombre de pneumonies à pneumocoque dues à l’un des 13 sérotypes inclus dans le vaccin Prevenar 13 dans le groupe des personnes vaccinées et dans le groupe témoin. L’efficacité dans le groupe des personnes vaccinées avec Prevenar 13 était de 46 %. Quand le critère d’efficacité comparait le nombre d’infections invasives à pneumocoque entre les deux groupes de personnes, l’efficacité était de 75 %.
Deux vaccins pneumococciques sont actuellement disponibles en France :
- Le vaccin conjugué 13-valent Prevenar 13, qui contient 13 sérotypes du pneumocoque,
- Le vaccin polyosidique non conjugué 23-valent Pneumo 23, qui contient 23 sérotypes du pneumocoque.
Le vaccin Pneumovax (vaccin polyosidique 23-valent non conjugué) possède également une autorisation de mise sur la marché en France où il a déjà été commercialisé, notamment en période de rupture de stock du vaccin Pneumo 23.
Vaccin conjugué 13-valent
L’efficacité du vaccin Prevenar 13 contre les pneumopathies à pneumocoque de sérotype vaccinal semble persister pendant au moins les quatre ans qui suivent la vaccination.
Mais chez les personnes vaccinées antérieurement avec le vaccin polyosidique non conjugué 23 valent, l’efficacité de Prevenar 13 est moindre si le délai entre les deux injections est court (moins d’un an). Il faut ainsi un délai d’au moins un an entre l’administration de la dose d’un vaccin 23-valent et celle du vaccin Prevenar 13 pour ne pas observer d’hyporéponse immunitaire.
Les données médico-économiques ont également été prises en compte pour choisir une stratégie coût-efficace d’utilisation des vaccins 13-valent et 23-valent chez les personnes à risque d’infection à pneumocoque.
Vaccin polyosidique non conjugué 23-valent
L’intérêt du vaccin polyosidique 23-valent est d’élargir la protection à d’autres sérotypes du pneumocoque que ceux qui sont inclus dans le vaccin Prevenar 13. En 2015, en analysant les sérotypes des souches de pneumocoques responsables d’infections invasives (réseau Epibac), 58 % des pneumocoques non inclus dans le vaccin Prevenar 13 étaient couverts par le vaccin polyosidique 23-valent.
L’efficacité du vaccin polyosidique 23-valent a été montrée dans la prévention des infections invasives à pneumocoque. Cependant, l’efficacité vaccinale contre les pneumopathies dues à des pneumocoques de sérotype vaccinal, et contre les pneumopathies communautaires en général, est moins élevée.
L’immunogénicité du vaccin polyosidique non conjugué 23-valent est limitée dans le temps car les anticorps protecteurs ne sont plus détectables 2 à 6 ans après l’administration du vaccin. Ainsi, chez les personnes de 65 ans et plus, l’efficacité du vaccin sur le terrain est de 65 % deux ans après l’administration de la dose vaccinale.
Au-delà de cinq ans, le vaccin ne semple plus conférer une protection. Mais les revaccinations successives avec un vaccin polyosidique non conjugué 23-valent, lorsqu’elles sont réalisées avec un intervalle court (moins de 6 mois), ne permettent pas d’augmenter la réponse immunitaire : ces revaccinations itératives entrainent au contraire une hyporéactivité (c’est-à-dire une moindre réponse immunologique).
Cette hyporéactivité disparaît avec le temps. De plus, la survenue d’effets indésirables est significativement plus fréquente en cas de revaccination dans un délai inférieur à 5 ans.
Ainsi, un délai d’au moins 5 ans entre deux doses de vaccin polyosidique 23-valent est recommandé.
En résumé, le vaccin Prevenar 13 est plus efficace que le vaccin Pneumo 23, mais il contient 10 sérotypes de moins.
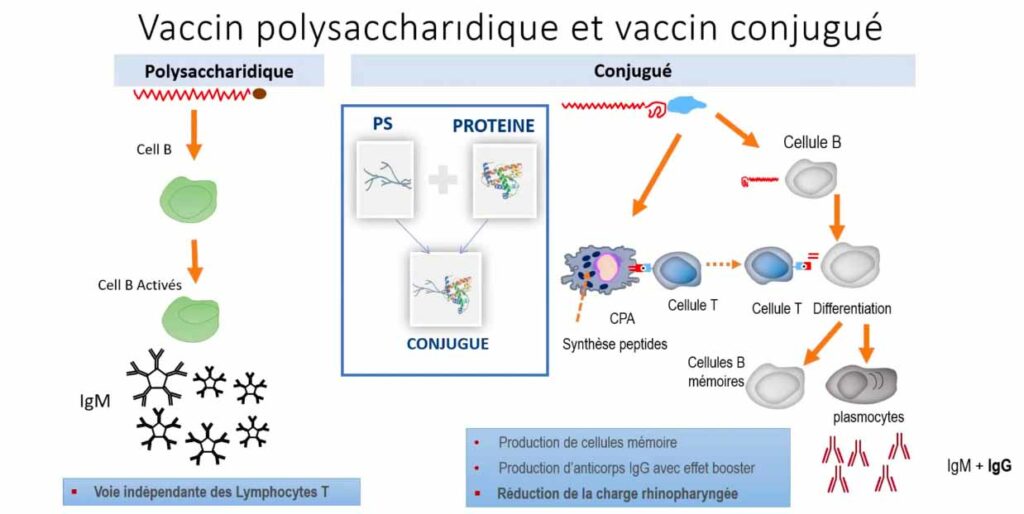
Sources : Ada G. N Engl J Med. 2001 ;345 :1042-1053.
OverturfGD, Committee on Infectious Diseases. Pediatrics. 2000;106:367-376.
Effet direct et indirect de la Vaccination des enfants :
Evolution du taux d’incidence des infections invasives à pneumocoques selon l’âge et de la couverture vaccinales à 24 mois en France métropolitaine de 2001 à 2016.
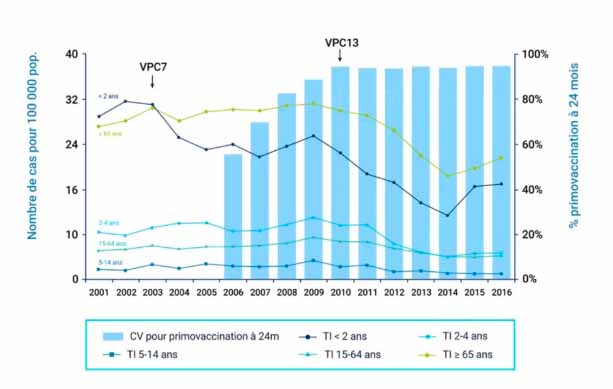
Sources : Epibac, Echantillon généraliste des bénéficiaires, estimations Santé publique France
Nouvelles recommandations vaccinales 2017 antipneumococciques :

En plus de la prévention des infections invasives à pneumocoque (méningites et septicémies), les recommandations vaccinales sont maintenant justifiées en outre par la prévention des pneumopathies. Ceci a entraîné une modification du chapitre correspondant du calendrier vaccinal, qui s’intitulait « Infections invasives à pneumocoque (IIP) » et s’intitule maintenant « infections à pneumocoque (IP) ».
Dans l’objectif d’obtenir une réduction de la fréquence des pneumonies et des infections invasives à pneumocoque, le schéma vaccinal recommandé en 2013 pour les adultes immunodéprimés est maintenant étendu aux adultes de tous âges non immunodéprimés à risque élevé d’infection invasive et de pneumonie à pneumocoque. Ce schéma est le suivant :
Une dose de vaccin 13-valent Prevenar 13 ;
Puis une dose de vaccin 23-valent Pneumo 23 deux mois plus tard.
Auparavant, chez les personnes à risque non immunodéprimées, une dose unique de vaccin 23-valent était recommandée. Désormais, le schéma vaccinal est donc identique pour tous les adultes à risque. Le calendrier vaccinal 2017 précise également que ce schéma est applicable à partir de l’âge de 5 ans.
Des précisions sont apportées sur la conduite à tenir en fonction de l’historique vaccinal. Pour les personnes ayant reçu antérieurement une dose de vaccin 23-valent, il est recommandé d’administrer une dose du vaccin Prevenar 13 au moins un an après (au lieu de trois ans dans la précédente recommandation), puis à nouveau une dose de vaccin 23-valent 5 ans après la dose précédente de 23-valent.
Pour les personnes ayant déjà été vaccinées avec le vaccin Prevenar 13 puis un vaccin 23-valent, une deuxième dose de vaccin 23-valent est recommandée après un délai d’au moins 5 ans.
La nécessité de revacciner ultérieurement avec des doses supplémentaires de Prevenar 13 ou avec un vaccin 23-valent n’a pas été évaluée.
Couvertures vaccinales de patients à risques
L’objectif de l’étude Covarisq était de déterminer le Taux de vaccination anti-grippale (AG) et antipneumococcique (AP) chez les personnes immunodéprimées et atteintes de BPCO, affiliées à l’assurance maladie, à partir du Système National des Données de Santé (SNDS) entre le 1er janvier 2014 et le 31 décembre 2018.
Les recommandations françaises préconisaient une vaccination systématique antigrippale (AG) – Voir Chapitre Grippe – et antipneumococcique (AP) chez les personnes atteintes de BPCO quelle que soit la sévérité de la maladie.
Par VPP-23 tous les 5 ans avant 2017, puis par VPC-13 suivi 8 semaines plus tard d’un VPP-23, le schéma VPC-13 puis VPP-13 étant recommandé depuis 2014 chez les immunodéprimés.
Entre 2014 et 2018, le nombre de personnes identifiées « BPCO » a augmenté de 2%, passant de 603 257 à 616 003 personnes.
Concernant les personnes BPCO, en 2017, seulement 29% des malades étaient à jour de leur vaccination VPP-23.
En 2018 le taux cumulé de vaccination (AG + AP) était de 37% (athme, BPCO et emphysèmes), la tranche d’âge supérieure à 65 ans étant presque 2 fois mieux vaccinée 41%) que celle inférieure ou égale à 45 ans (22%).
Pour les personnes vivant avec un diabète (2,5 millions de personnes – Voir chapitre prévention/HTA et Diabète/Diabète), le taux de couverture était seulement de 7%.
Concernant les immunodéprimés, le schéma à 2 doses (VPC13 + VPP-23) était recommandé :
- Depuis 2012 pour 3 groupes de personnes : Implants Cochléaires (taux de couverture vaccinale de 17 %), insuffisance rénale chronique terminale (taux de couverture vaccinale de 12 %) et brèche ostéo-méningée (taux de couverture vaccinale de 2 %).
- Depuis 2014, en cas de chimiothérapie pour tumeur solide ou pour hémopathie maligne (taux de couverture vaccinale de 6 %), en cas de syndrome néphrotique (hospitalisation) et déficit immunitaire héréditaire (taux de couverture vaccinale de 9 %), personnes transplantées d’organes (taux de couverture vaccinale de 14 %), personnes porteuses de VIH quel que soit le statut immunologique (taux de couverture vaccinale de 19 %), personnes sous immunossupresseurs ou biothérapies MAI ou MICI (taux de couverture vaccinale de 20 %).
En conclusion de cette étude, dans la population des malades atteints de BPCO et celle des immunodéprimés, les taux de vaccination AG et AP restaient très inssuffisants en 2017, particulièrement pour le pneumocoque.
Les efforts visant à corriger cette situation doivent s’intensifier ; la CPTS Var Ouest a pour objectif de s’attacher à cela.
Grippe
(ou inlfuenza)
La maladie
La grippe est une infection respiratoire aiguë causée par le virus influenza. Le mot « influenza » désigne d’ailleurs la grippe elle-même dans plusieurs langues (influenza di freddo signifiant « sous l’influence du froid » en italien). Quant au mot « grippe », il est probablement issu du francique « grip », qui signifie à la fois « ce qui saisit », illustrant le début brutal de la grippe, et « mésaventure »…
Il existe trois types de virus influenza, dénommés A, B et C. Seuls les virus A et B ont une importance épidémiologique, particulièrement le virus A en raison de sa variabilité, qui lui permet de déjouer les défenses immunitaires de l’homme.
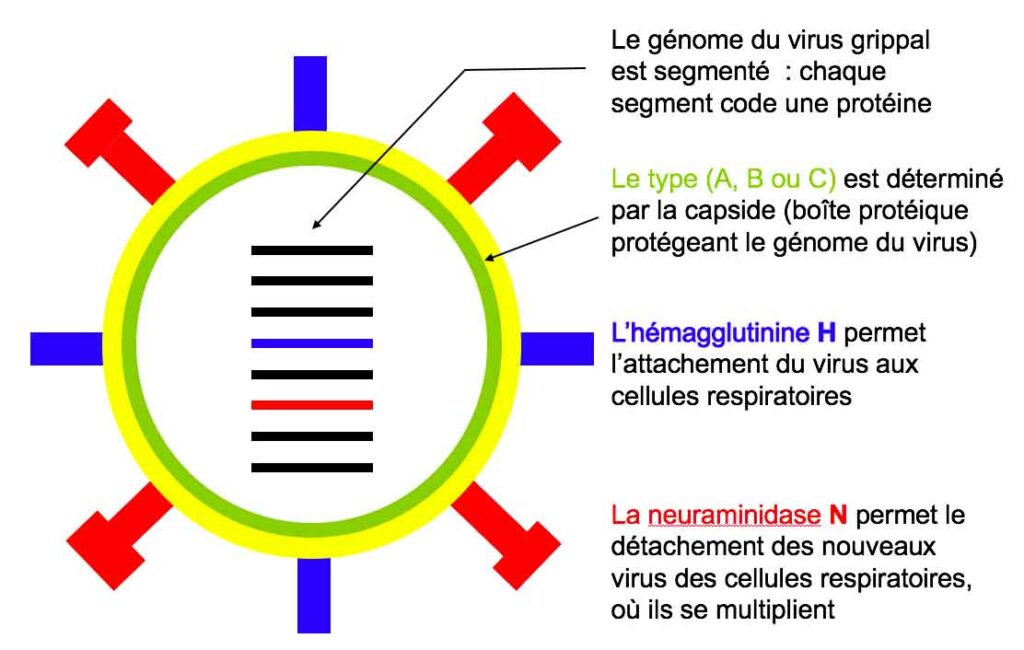
Le virus grippal possède à sa surface deux glycoprotéines antigéniques, l’hémagglutinine et la neuraminidase, désignées respectivement par les lettres H et N.
L’hémagglutinine permet l’attachement du virus aux cellules respiratoires et la neuraminidase permet la libération des virions néo-formés lors de leur sortie par bourgeonnement de la cellule infectée.
Chez les animaux, principal réservoir de virus influenza de type A, 18 sortes de H (H1 à H18), dont certaines découvertes en 2013, et 11 sortes de N (N1 à N11) ont été identifiées.
Le virus se transmet de personne à personne par voie respiratoire, par l’intermédiaire de particules de salive et surtout d’aérosols émis lors de la toux ou des éternuements. Une certaine résistance des virus grippaux dans le milieu extérieur explique la possibilité d’une transmission manuportée et donc l’importance du lavage des mains dans la lutte contre la transmission.
L’éducation des populations au lavage régulier et correct des mains est ainsi un élément important dans la lutte contre ce type de pathologie (tout comme la COVID, la Bronchiolite, ou la gastro-entérite, notamment)
Après une incubation de 24 à 48 heures, le début de la grippe est typiquement brutal et se caractérise par une fièvre élevée, des frissons, une asthénie intense, des courbatures, des céphalées, des douleurs diverses. On observe souvent des signes d’irritation laryngo-trachéale, bronchitique ou conjonctivale. Fièvre et douleurs durent trois ou quatre jours et la courbe thermique peut revêtir un aspect diphasique (le « V » grippal). Une guérison rapide est habituelle, mais la convalescence peut être longue, avec une asthénie persistante. La létalité (proportion de décès parmi les cas) peut être élevée aux âges extrêmes de la vie et chez les personnes atteintes de maladies chroniques : affections respiratoires, cardiovasculaires ou rénales chroniques, diabète… La gravité peut être due au virus lui-même (formes « toxiques ») ou aux surinfections bactériennes.
La plupart des cas de grippe saisonnière admis en réanimation sont des personnes âgées de 65 ans et plus ou souffrant de maladie chronique, ou des femmes enceintes.
Les enfants jouent un rôle important dans l’épidémiologie de la grippe. Le risque d’infection concerne en particulier les enfants d’âge scolaire et ceux vivant en collectivité. Le risque d’hospitalisation est maximal dans la première année de vie et est alors équivalent à celui des adultes à risque. Le risque de décès est dix fois plus élevé dans la tranche d’âge des 1-12 mois, avec un risque maximal pour les moins de 6 mois, par rapport à la tranche d’âge des 5-9 ans.
Les nourrissons de moins de 6 mois représentent une population à protéger en priorité du fait de risques de formes graves, d’hospitalisation et de décès, mais aussi parce que la vaccination n’est pas possible dans cette tranche d’âge.
Un tableau d’aspect grippal peut être provoqué par de nombreux agents infectieux, viraux ou non, et peut lui-même être très variable, de sorte que l’on ne peut identifier la grippe « vraie » qu’au laboratoire, surtout au début d’un épisode épidémique. L’aspect épidémique lui-même, si emblématique de la grippe, n’est pas rigoureusement constant et peut être provoqué par d’autres virus : Paramyxovirus parainfluenzae, adénovirus, virus respiratoire syncytial…
Les recommandations vaccinales
1.Vaccins disponibles.
Vaccins inactivés injectables.
Il existe trois types de vaccins grippaux inactivés cultivés sur oeuf embryonné de poule :
- A virus entier ;
- A virus fragmenté ;
- Sous-unités à antigène de surface.
Ces deux derniers sont de loin les plus utilisés, car moins réactogènes que les préparations à virus entier (dont il n’existe, du reste, pas de vaccin commercialisé en France).
Les vaccins à virions fragmentés (type VaxigripTetra et FluarixTetra, ce dernier n’étant plus disponible depuis la saison 2019-2020) sont constitués de particules obtenues après dissociation du virus par un détergent.
Les vaccins sous-unités à antigènes de surface (type Influvac et Influvac TetraA) sont composés de neuraminidase et d’hémagglutinine virales purifiées après élimination des autres constituants.
Depuis décembre 2018, il faut ajouter un autre type de vaccin inactivé injectable à antigènes de surface : il s’agit d’un vaccin obtenu à partir de virus multipliés sur culture de cellules de rein de chien (MDCK). Ce vaccin (Flucelvax tetra) ne contenant pas de traces de protéines d’oeuf ou d’antibiotiques, il peut être utilisé chez les personnes allergiques à ces produits (avis de la HAS d’octobre 2019) à partir de l’âge de 9 ans.
Le vaccin VaxigripTetra est le seul vaccin disponible en France au moment où est rédigé cet article qui pourra être utilisé chez les nourrissons âgés de six mois à deux ans révolus.
Vaccin vivant atténué
Le vaccin vivant atténué contre la grippe Fluenz Tetra (utilisable de l’âge de 24 mois à 17 ans révolu), administré par voie nasale, n’est pas disponible en France.
2. Recommandations vaccinales.
Ces recommandations sont basées sur les avis du Haut Conseil de santé publique du 23 avril 2010, du 25 juin 2010, du 24 septembre 2010, du 29 décembre 2010, du 17 décembre 2010, du 13 juillet 2011, du 21 octobre 2011, du 16 février 2012 et du 22 février 2013.
Une campagne de vaccination est lancée chaque année avant la saison hivernale.
Le vaccin est intégralement pris en charge par l’Assurance Maladie sans avance de frais pour les personnes chez lesquelles existent des recommandations vaccinales :
Les recommandations générales
Personnes âgées de 65 ans et plus.
Les recommandations particulières
Personnes, y compris les enfants à partir de l’âge de 6 mois et les femmes enceintes*, atteintes d’une des pathologies suivantes :
- Affections broncho pulmonaires chroniques répondant aux critères de l’ALD 14 (asthme et bronchopneumopathie chronique obstructive ou BPCO) ;
- Insuffisances respiratoires chroniques obstructives ou restrictives quelle que soit la cause, y compris les maladies neuromusculaires à risque de décompensation respiratoire, les malformations des voies aériennes supérieures ou inférieures, les malformations pulmonaires ou les malformations de la cage thoracique ;
- Maladies respiratoires chroniques ne remplissant pas les critères de l’ALD mais susceptibles d’être aggravées ou décompensées par une affection grippale, dont asthme, bronchite chronique, bronchiectasies, hyper-réactivité bronchique ;
- Dysplasie broncho-pulmonaire (traitée au cours des six mois précédents par ventilation mécanique, oxygénothérapie prolongée ou traitement médicamenteux continu par corticoïdes, bronchodilatateurs ou diurétiques) ;
- Mucoviscidose ;
- Cardiopathies congénitales cyanogènes ou avec une hypertension artérielle pulmonaire ou une insuffisance cardiaque ;
- Insuffisances cardiaques graves ;
- Valvulopathies graves ;
- Troubles du rythme graves justifiant un traitement au long cours ;
- Maladies des coronaires ;
- Antécédents d’accident vasculaire cérébral ;
- Formes graves des affections neurologiques et musculaires (dont myopathie, poliomyélite, myasthénie, maladie de Charcot) ;
- Paraplégie et tétraplégie avec atteinte diaphragmatique ;
- Néphropathies chroniques graves ;
- Syndromes néphrotiques ;
- Drépanocytoses, homozygotes et doubles hétérozygotes S/C, thalassodrépanocytose ;
- Diabète de type 1 et de type 2 ;
- Déficit immunitaire primitif ou acquis (pathologies oncologiques et hématologiques, transplantation d’organe et de cellules souches hématopoïétiques, déficits immunitaires héréditaires, maladies inflammatoires ou auto-immunes recevant un traitement immunosuppresseur), excepté les personnes qui reçoivent un traitement régulier par immunoglobulines, sujets infectés par le VIH quels que soient leur âge et leur statut immunovirologique ;
- Femmes enceintes sans facteur de risque spécifique (dès le premier trimestre de grossesse)
- Personnes obèses (indice de masse corporel supérieur ou égal à 40)
- Personnes atteintes d’une hépatopathie chronique, avec ou sans cirrhose*.
- Personnes séjournant dans un établissement ou service de soins de suite ainsi que dans un établissement médico-social d’hébergement, quel que soit leur âge.
- Entourage familial des nourrissons âgés de moins de 6 mois présentant des facteurs de risque de grippe grave ainsi définis : prématurés, notamment ceux porteurs de séquelles à type de broncho dysplasie (traitée au cours des six mois précédents par ventilation mécanique, oxygénothérapie prolongée ou traitement médicamenteux continu par corticoïdes, bronchodilatateurs ou diurétiques) et enfants atteints de cardiopathie congénitale, de déficit immunitaire congénital, de pathologie pulmonaire, neurologique ou neuromusculaire ou d’une affection de longue durée.
- L’entourage des personnes immunodéprimées (nouveauté 2019).
- Pour les femmes sans facteur de risque spécifique qui accouchent durant la période de circulation virale, et dont l’enfant présente des facteurs de risque, une vaccination est recommandée et devrait être pratiquée à la maternité.
- Les recommandations professionnelles
- Professionnels de santé et tout professionnel en contact régulier et prolongé avec des sujets à risque de grippe sévère ;
- Personnel navigant des bateaux de croisière et des avions et personnel de l’industrie des voyages accompagnant les groupes de voyageurs (guides).
Améliorer la couverture vaccinale : objectif de l’OMS : 75% de la population
En France, la couverture vaccinale (taux cumulé) est inférieure à 52 % chez les 65 ans et plus et de 35 % chez les moins de 65 ans à risque.
La CPTS Var Ouest va donc mener des actions de prévention primaire (visant à diminuer l’incidence d’une maladie dans la population et à réduire les risques d’apparition de nouveaux cas par la diminution des causes et des facteurs de risque) d’une part, et des actions de prévention secondaire d’autre part (visant à diminuer la prévalence d’une maladie dans la population par la détection et le traitement précoce via notamment l’orientation vers le professionnel adéquat), notamment à travers la vaccination.
Pour cela, la CPTS va promouvoir la vaccination en général auprès de l’ensemble de la population territoriale en s’appuyant notamment sur les campagnes nationales que réalisent les différents acteurs de santé publique (Assurance Maladie, ARS, Gouvernement, etc.)
La CPTS est par définition, « facilitatrice de santé », facilitatrice d’accès aux soins.
Ainsi, la stratégie autour de la vaccination peut se synthétiser sous la forme :
″Améliorer l’information et faciliter la réalisation″
Un exemple instructif est celui des femmes enceintes :
Selon l’enquête nationale périnatale de l’INSERM (2016), elles sont très peu vaccinées (7,4%).
La vaccination est très peu proposée :
- Gynécologues : 36%
- Médecins généralistes : 32 %
- Sages-femmes : 13 %
Lorsqu’elle est proposée, dans 70 % des cas elle est refusée par peur du vaccin pour la grossesse et le bébé.
Les campagnes de communication et la persuasion sont donc des arguments insuffisants.
Lire l’étude nationale périnatale de l’INSERM (2016)
Moyen d'y remédier
1/ Organisation : 248 femmes enceintes de 3 maternités de l’AP-HP (Port-Royal, Louis Mourier, Bichat) ont participé à un protocole dédié à la vaccination.
La disponibilité du vaccin sur place multipliait par 25 le recours à la vaccination.
Lire l’étude issue du protocole
2/ Information (et non pas communication) : Expérimentation au CHU de Lille sur plus de 2000 femmes sur la saison 2014-2015.
Il apparaît que l’état des connaissances est moyen. 40 % des femmes incluses dans l’expérimentation ne connaissent pas les risques d’une grippe durant la grossesse, 10 % pensent que le vaccin est contre-indiqué et 48 % pensent qu’il y a un risque d’effets iatrogènes pour l’enfant.
Un haut niveau de connaissance permet de multiplier par 3 l’acceptation et le recours à la vaccination.
Lire l’étude menée au CHU de Lille
La vaccination, en France, est intégralement prise en charge et sans aucune avance de frais pour les personnes à risques et femmes enceintes. Un bon de prise en charge pour la vaccination antigrippale est adressé, chaque année, à 12 millions de personnes ; Environ 50 % seulement sont utilisés.
La vaccination peut faire l’objet d’une prescription ET être réalisée par un médecin ou une sage-femme
Elle peut également être réalisée sans prescription médicale préalable par un infirmier ou un pharmacien (maillage territorial important)
Plusieurs axes et orientations sont envisagés dans le projet de santé :
- Soutenir l’intervention des médecins généralistes relativement à la vaccination par une intervention partagée
- Augmenter le taux de vaccination des soignants contre la grippe saisonnière et toute autre vaccination.
- Faciliter l’acte de vaccination par l’ensemble des professionnels de santé habilités (médecins traitants, IDEL, pharmaciens, sages-femmes) en informant la population des possibilités offertes et en leur offrant les conditions matérielles propices (mise à disposition de lieu de vaccination ou de moments spécifiques)
- Rattraper les éventuels retards de vaccination dus à la crise Covid-19
VACCINATION et COVID
Depuis le 15 mars 2021, le territoire de la CPTS Var Ouest a vu s’ouvrir un centre de vaccination COVD sur la Commune du Beausset co-géré par la CPTS Var Ouest => Lien vers COVID/Cendre de vaccination Le Beausset.
Des centres de vaccination éphémères ont également vu le jour sur les communes de Six-Fours-Les-Plages (du 26 mars au 02 avril 2021 et Sanary-Sur-Mer du 27 au 30 avril 2021 pour la première injection de vaccin)
Nous vous proposons un document ayant pour but d’accompagner les soignants afin de mieux répondre aux questions de la population.
Pour permettre la réussite de ce projet ambitieux, la CPTS Var Ouest envisage de miser sur la communication, tant auprès des professionnels de santé que de la population territoriale.
La CPTS va créer à cet effet une revue de la CPTS, gratuite (financement par des annonceurs), distribuée à la population par mise à disposition d’exemplaires chez les professionnels de santé.